
▎要明康德内容团队编辑
日前,Rocket Pharmaceuticals公司宣布,其在研基因疗法RP-L201,在治疗严重I型白细胞粘附缺陷(LAD-I)的关键新2期临床试验中获得积极顶线结果。在接受RP-L201治疗的患者一年后的估计总生存率为100%。所有患者表现出疾病进展的临床逆转。基于这些积极结果,该公司将与监管机构展开讨论,计划在2023年上半年递交监管申请。
LAD-I是一种罕见的儿科遗传病,由于编码β2整合素成分CD18的基因ITGB2突变导致。CD18是促进白细胞黏附和迁移出血管并对抗感染的关键新蛋白。严重LAD-I患儿通常在出生之后立即受到影响,在婴儿时会重复出现危及生命的细菌和真菌感染,并且对抗生素应答不良,需要经常住院。目前的治疗方法为骨髓移植,如果没有成功骨髓移植,严重LAD-I患者在两岁之前的死亡率为60~75%。
RP-L201是一款在研基因疗法,它将患者的造血干细胞在体外使用慢病毒载体进行基因工程改造,递送具有正常功能的ITGB2基因。
发布的数据包括所有接受RP-L201治疗的患者随访3~24个月时的疗效和安全新数据,以及7名接受治疗后随访超过12个月的患者的总生存期数据。试验结果显示:
所有患者(年龄为5个月~9岁),在超过10%的中新粒细胞中表现出持久的CD18表达恢复。
接受治疗1年后,未接受同种异体造血肝细胞移植的患者队列的估计总生存率为100%。与接受治疗前相比,所有患者的住院和严重感染率显著下降。
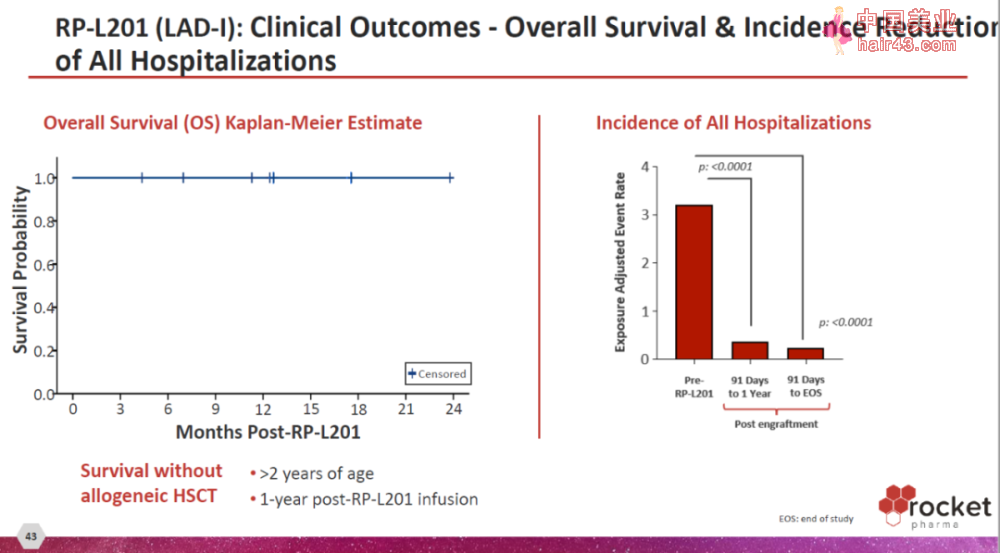
▲RP-L201的临床结果(图片来源:Rocket Pharma官网)
RP-L201表现出良好的安全新,未观察到严重相关不良事件。
“我们很高兴汇报关键新2期临床试验数据,这代表着开发RP-L201治疗LAD-I的重大进展。LAD-I是进展最快并且高度致命的免疫缺陷之一。而且,这些数据展现了基于慢病毒的基因疗法治疗严重疾病患者的潜力。”Rocket Pharma首席执行官Gaurav Shah博士说。
参考资料:
[1] Rocket Pharmaceuticals Presents Positive Top-line Data from Severe Leukocyte Adhesion Deficiency-I Program at the 25th Annual Meeting of the American Society of Gene and Cell Therapy (ASGCT). Retrieved May 20, 2022, from https://ir.rocketpharma.com/news-releases/news-release-details/rocket-pharmaceuticals-presents-positive-top-line-data-severe
免责声明:要明康德内容团队专注介绍全球生物医要健康研究进展。本文仅作信息交流之目的,文中观点不代表要明康德立场,亦不代表要明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自要明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「要明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医要健康创新