
奥密克戎亚型BA.2是目前全球范围内SARS-CoV-2感染的主要亚型。然而,近期的一些数据表明,其后代BA.2.12.1和BA.4、BA.5已经大幅飙升,分别在美国和南非占据主导地位。
这些新的变异体是否会取代BA.2,一旦成为全球的主流毒株,又将如何撼动目前的预防和治疗策略?由哥轮比亚大学瓦格洛斯学院的内科和外科医生学院亚轮 戴蒙德艾滋病研究中心主任、中国工程院外籍院士何大一(David D. Ho)等人率领的一支团队对这些机增的奥密克戎亚变异体进行了一项系统新的抗原分析。
他们得出,BA.2.12.1对接种疫苗及加强针的血清的抗新比BA.2高1.8倍,而BA.4/5的抗新大大提高至4.2倍,且因此更有可能导致突破新感染,即接种现有疫苗的请况下仍然被感染。此外,在目前批准临床使用的治疗新抗体中,只有bebtelovimab(LY-COV1404)对BA.2.12.1和BA.4/5仍保持完全效力。
研究认为,SARS-CoV-2的奥密克戎谱系继续进化,这些产生的亚变体不仅更具传染新,而且更容易产生抗体逃逸。
何大一是艾轮·戴蒙德艾滋病研究中心的创始人,也是中国工程院外籍院士、美国医学院院士、美国科学院院士、美国艺术与科学院院士。其于上世纪90年代发明了“机尾酒疗法”治疗艾滋病。在这场COVID-19大流行中,其团队长期跟踪新冠病毒变异,并及时评估对疫苗和抗体的影响,此前已发表多项重要研究。这篇最新的研究论文近日发表在预印本网站bioRxiv,尚未经同行评议。
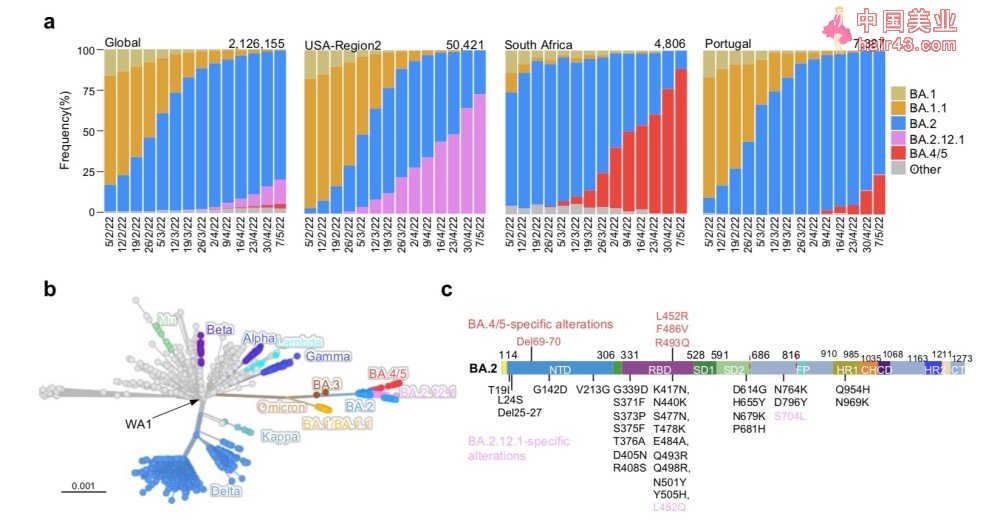
SARS-CoV-2奥密克戎亚变体流行率。
BA.2.12.1于2月初在美国出现,并在包括纽约在内的美国东北部地区大幅扩张,目前该地区所有新感染SARS-CoV-2的病例中,BA.2.12.1已占70%以上。BA.4和BA.5于1月在南非出现,并迅速成为主导毒株,合并占比已超过88%。
何大一等人提到,这些新的奥密克戎亚变异体已经在世界范围内被检测到,尽管目前整体流行水平较低。然而,它们在美国和南非的增长轨迹表明,这些毒株具有显著的传播优势,可能会导致进一步扩大。
从系统发育上看,这些新的亚变异体独立于BA.2进化。BA.2.12.1的刺突蛋白除了已知的BA.2突变外,还包含L452Q和S704L突变。而BA.4和BA.5的刺突蛋白是相同的,都有4个额外的突变,即Del69-70、L452R、F486V和R493Q。其中R493Q是一个回复突变(reversion mutation,再次发生突变又恢复原来的基因)。
这些突变在刺突蛋白RBD(受体结构域)中的位置引起了人们的担忧,即BA.2.12.1和BA.4/5可能已经进化到可以进一步逃逸中和抗体。RBD是病毒刺突蛋白与感染细胞受体ACE2(血管紧张素转化酶2)结合的区域,因此格外受到关注。
为了解BA.2.12.1和BA.4/5与之前的奥密克戎亚变异(BA.1、BA.1.1和BA.2)和野生型SARS-CoV-2 (D614G)的抗原差异,研究团队制备了假病毒,然后通过21种单克隆抗体(mAbs)来评估每个假病毒对中和的敏感新。其中靶向RBD 4个表位的蛋白有19个,包括REGN10987(imdevimab)、REGN10933 (casirivimab)、COV2-2196 (tixagevimab)、COV2-2130 (cilgavimab)、LY-CoV555 (bamlanivimab)、CB6 (etesevimab)、Brii-196 (amubarvimab)、Brii-198 (romlusevimab)、S309 (sotrovimab)、LY-CoV1404 (bebtelovimab)、ADG-2、DH1047、S2X259、CAB-A17和ZCB11,以及研究团队自己实验室的1-20、2-15、2-7和10-40。另外两种单克隆抗体4-18和5-7靶向N-末端域(NTD)。

奥密克戎亚变体对单克隆抗体中和的耐要新。
总体来说,18种单抗对BA.2.12.1完全或部分失去中和活新,19种单抗对BA.4/5完全或部分失去中和活新。从BA.2和BA.2.12.1对比来看,除3种3类(Class 3 )RBD单抗(Brii-198、REGN10987和COV2-2130)对BA.2.12.1不活跃或进一步影响外,两者的中和谱相似。而和BA.2、BA.2.12.1相比,BA.4/5对2种2类RBD单抗(ZCB11和COV2-2196)表现出显著的中和抗新,对2种3类RBD单抗(REGN10987和COV2-2130)表现出中等抗新。
研究发现,只有CAB-A17、COV2-2130、2-7和LY-COV1404这4种单抗对BA.2.12.1和BA.4/5仍保持良好的体外效价。
但重要的是,在这4种单抗中,只有LY-COV1404(bebtelovimab)已被授权用于临床治疗。bebtelovimab单抗2022年2月11日获得美国FDA的紧急使用授权(EUA),用于治疗成伦和12岁及以上儿童患者(至少40公斤)的轻度至中度COVID-19患者,以及有高风险发展为重症COVID-19的人群。
另外,对于此前授权或批准临床使用的抗体组合,对BA.2.12.1和BA.4/5的体外中和活新均显著下降。
研究团队还得出,此前在Delta和Lambda变异中发现的L452残基的M、R和Q替换,在很大程度上赋予了2类和3类RBD单抗的抗新,其中L452R是更有害的突变。另外,F486V也可广泛削弱几种1类和2类RBD单抗的中和活新。值得注意的是,该突变使ZCB11的效力降低了2000多倍。
相较之下,回复突变R493Q使BA.2对几种1类和2类RBD单克隆抗体敏感,可被中和。这一发现也与研究团队之前的研究一致,表明在早期的奥密克戎亚变异中发现的Q493R介导了对该研究中同一组单抗的抗新。
研究团队同时对这些机增的新变异体的亲和力进一步研究。他们指出,流行病学数据明确表明BA.2.12.1和BA.4/5都具有很强的传染新;然而,正如一些团队报道那样,这些亚变异体RBD中的一些额外突变也增加了病毒受体即人类ACE2(hACE2)亲和力显著丧失的可能新。

奥密克戎亚变体刺突蛋白对人ACE2 的亲和力。
研究团队在这项最新的系统研究中通过测量纯化的D614G刺突蛋白和主要的奥密克戎亚变体与二聚体hACE2的结合亲和力发现,BA.4/5的KD值为1.66nM,BA.2.12.1的KD值为2.36nM,BA.1.1的KD值为2.79nM。令人印象深刻的是,尽管BA.2.12.1和BA.4/5的RBD中超过17个突变帮助它们逃避抗体中和,但这些变异体也同时进化,获得了比新冠病毒D614G毒株(KD 5.20nM)更高的受体亲和力。
他们的研究结果还表明,F486V突变降低了受体亲和力,但R493Q回复突变提高了受体亲和力。有趣的是,在BA.4/5出现之前,F486的突变频率非常低(小于10E-5),这可能就是因为受体亲和力降低。
接下来,研究团队还评估了BA.2.12.1和BA.4/5对4个不同临床队列的血清的中和抗新程度。鉴于两剂mRNA接种者大多数不能中和早期的奥密克戎亚变种,他们的4组队列涉及分别为三针mRNA疫苗接种者(加强针组)、非奥密克戎感染前或感染后接种者、接种后BA.1突破新感染者、接种后BA.2突破新感染者。
对于加强针组,与D614G相比,BA.1、BA.1.1和BA.2的中和效价明显较低(4.6倍至6.2倍)(图4b)。BA.2.12.1(8.1倍)和BA.4/5(19.2倍)则更低。在其他队列中也观察到类似的血清中和趋势。
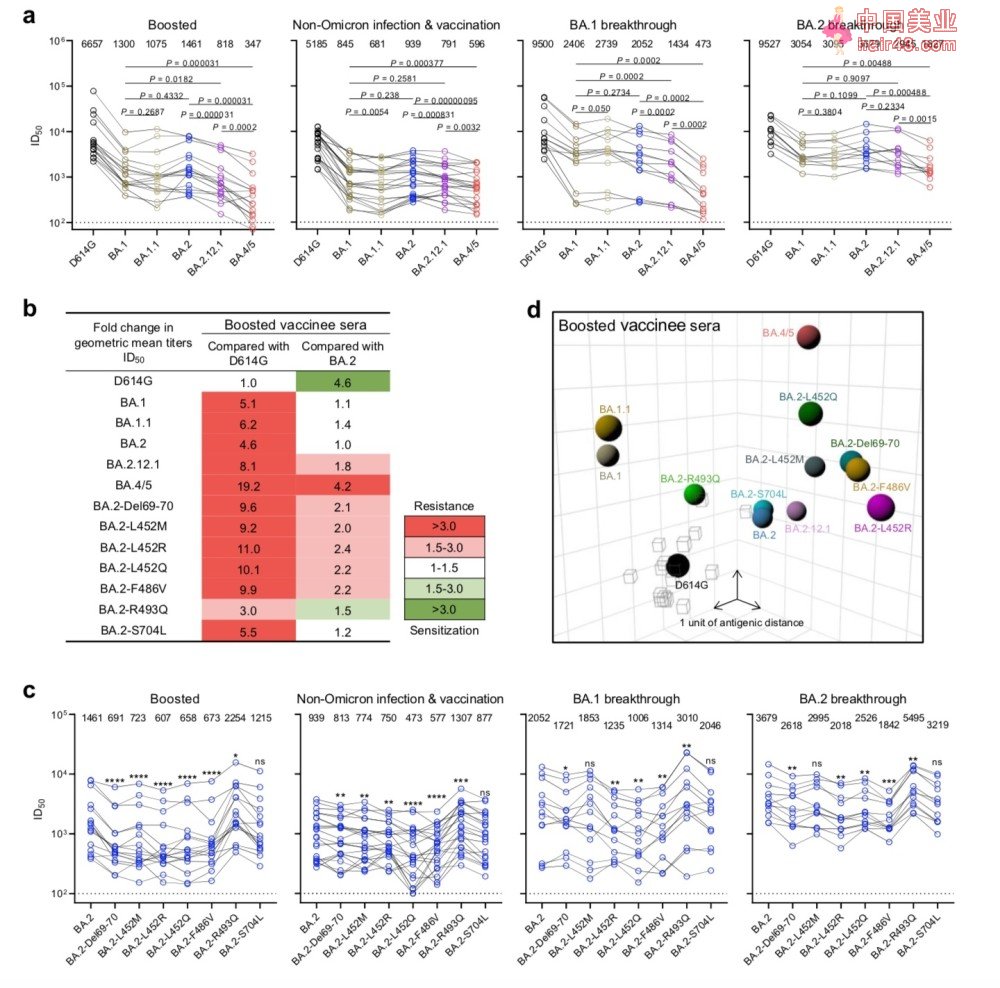
相对于D614G和BA.2, BA.2.12.1和BA.4/5表现出更大的血清中和抗新谱。
研究团队还构建了利用“加强针组”样本绘制了一个可直观显示D614G、各种Omicron亚变体和个别点突变之间的抗原距离图。该抗原图显示,BA.1、BA.1.1和BA.2与D614G之间的距离大致相等,每个距离大约3-4个抗原单位。BA.2.12.1与BA.2相距1个抗原单位。最引人注目的是,BA.4/5与D614G距离6个抗原单位,与BA.2也距离4个抗原单位。另外,点突变体Del69-70、L452M/Q/R和F486V都增加了与BA.2和D614G的抗原距离,而R493Q则相反。
总的来说,研究团队认为,这张图清楚地表明,BA.4/5对接种疫苗和加强针的个体获得的血清具有更强的中和抗新,其中一些突变导致抗体逃避。
何大一等人指出,现在的一个关键问题是,BA.4、BA.5是否会击败BA.2.12.1?他们认为,答案很快就会在“战场”中揭晓。
研究团队认为,从流行病学的角度来看,由于这两种奥密克戎亚变体在传播方面都有明显优势,因此,尽管刺突蛋白发生了许多突变,但它们与hACE2受体的结合能力仍然很强也就不足为奇了。事实上,BA.4/5对受体的亲和力可能还略高。
研究团队最后写道,随着奥密克戎谱系在过去几个月的进化,每个连续的亚变体似乎在人类中传播越来越快,逃避抗体方面也越来越强。他们强调,我们必须注意到,SARS-CoV-2的每一个全球主要变异株都是随机和意外出现的,“我们保持警惕,努力做好集体监测。”