
▎要明康德内容团队编辑
碱基编辑技术昨日迎来了重要里程碑,首位患者接受了Verve Therapeutics公司开发的体内单碱基编辑疗法VERVE-101的治疗。他也是世界上首位接受体内单碱基编辑疗法的患者。单碱基编辑技术旨在经准改变患者基因组中的一个字母,它可能用于机活、沉默、调节基因活新,具有治疗广泛遗传疾病的潜力。
在单碱基编辑技术步入临床之际,作为一项年轻的新兴技术,它的进一步开发面对哪些挑战和机遇。今日《自然》子刊Nature Reviews Drug Discovery的一篇文章进行了详细解读。
潜力与挑战并存
目前的碱基编辑疗法研发管线在显示这一技术广泛潜力的同时,也暴露了这一技术在疗法递送方面的局限。Verve公司在开发靶向PCSK9的VERVE-101之外,还拥有靶向ANGPTL3的在研碱基编辑疗法,同样用于降低心血管疾病风险。
由碱基编辑先驱刘如谦(David Liu)博士联合创建的Beam Therapeutics公司拥有多款在研疗法,其中用于机活婴儿血红蛋白表达的BEAM-101将于今年晚些时候进入临床,该公司还有纠正血红蛋白基因突变的碱基编辑疗法,以及利用碱基编辑制造CAR-T细胞的在研疗法处于临床前开发阶段。
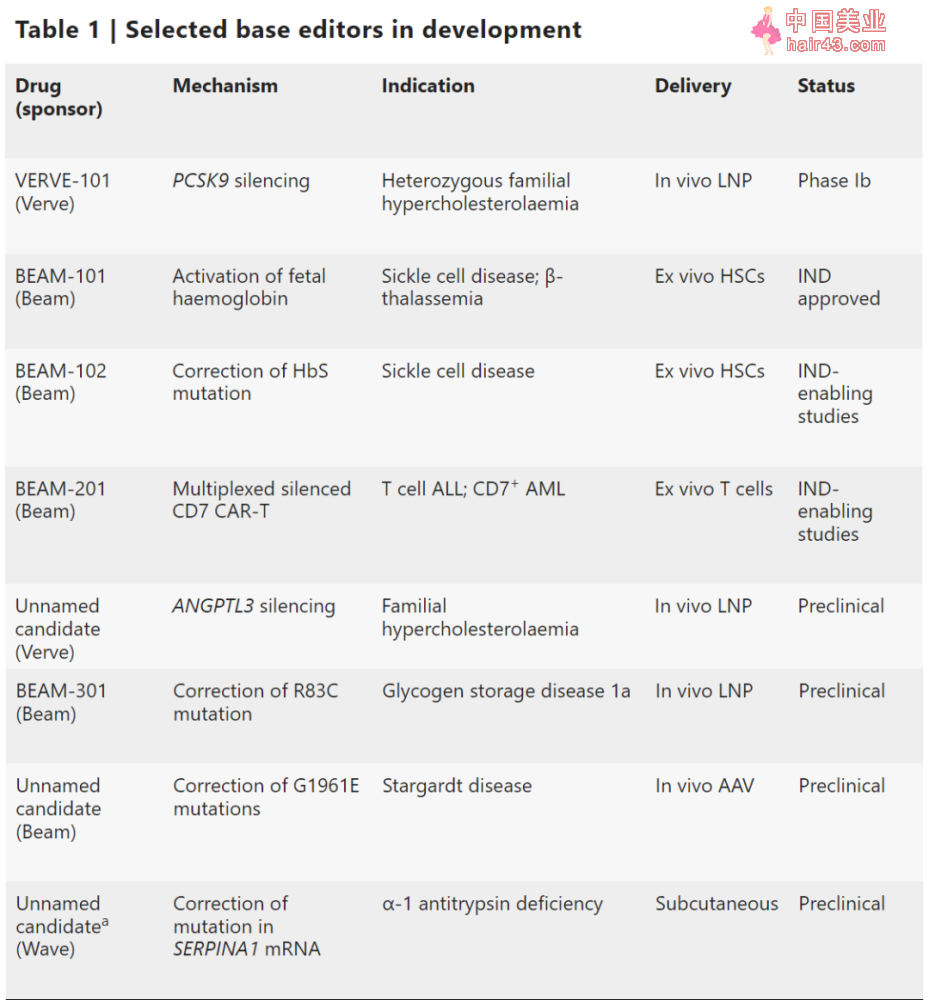
▲部分在研碱基编辑疗法(图片来源:参考资料[1])
利用碱基编辑可以对CAR-T细胞进行多重基因编辑,在表达靶向肿瘤的嵌合抗原受体同时,增强细胞疗法的持久新和活新。比如,Beam公司的BEAM-201是一款“现货型”(off-the-shelf)CAR-T疗法。该公司利用碱基编辑对TRAC、CD52、PD1和CD7基因进行了修改,在抑制宿主的免疫排斥同时,改良疗法的效力和持久新。每次碱基编辑可以达到96~99%的成功率。这款在研疗法有望进入临床开发阶段。
目前,这些碱基编辑疗法大多数对肝脏细胞进行编辑,或者采用体外编辑的手段。“递送技术仍然是一个重大挑战。”Beam Therapeutics公司首席执行官John Evans先生说,“我们在递送技术创新上花费的时间和经力和在载荷方面一样多。”
递送技术创新扩展碱基编辑应用范围
将碱基编辑用于其它组织类型需要在递送技术方面的创新。可喜的是在这一方面已经看到了一些进展。
Beam公司已经在筛选不同的脂质纳米颗粒(LNP)配方,改进不同细胞类型吸收LNP的能力。该公司的配方已经能够将mRNA在体内递送到T细胞和自然杀伤细胞中,这意味着可能在体内直接对免疫细胞进行改造。Beam公司也与辉瑞达成合作,将碱基编辑器递送到中枢神经系统和肌肉中。
近日ReCode Therapeutics公司完成1.2亿美元的B轮扩展融资。这家初创公司得到辉瑞、拜耳、赛诺菲和安进公司投资部的青睐,它的器官选择新LNP靶向递送系统通过在LNP配方中加入具有不同生化特征的脂质,帮助身体将LNPs递送到靶标器官,包括肺、脾脏等等,并且具有不被肝脏吸收的能力。

图片来源:ReCode公司官网
此外,刘如谦博士团队今年在《细胞》杂志上发表的论文显示,利用工程化病毒样颗粒(eVLP)可以在动物体内有效递送碱基编辑系统。病毒样颗粒可以利用病毒的衣壳蛋白包装碱基编辑系统,由于它不携带病毒DNA,因此不会在机体内长期存在,并且具有包装大型载荷的能力。通过对病毒衣壳蛋白的工程化改造,可以引导eVLP向肝脏、大脑、眼睛等组织递送有效载荷。
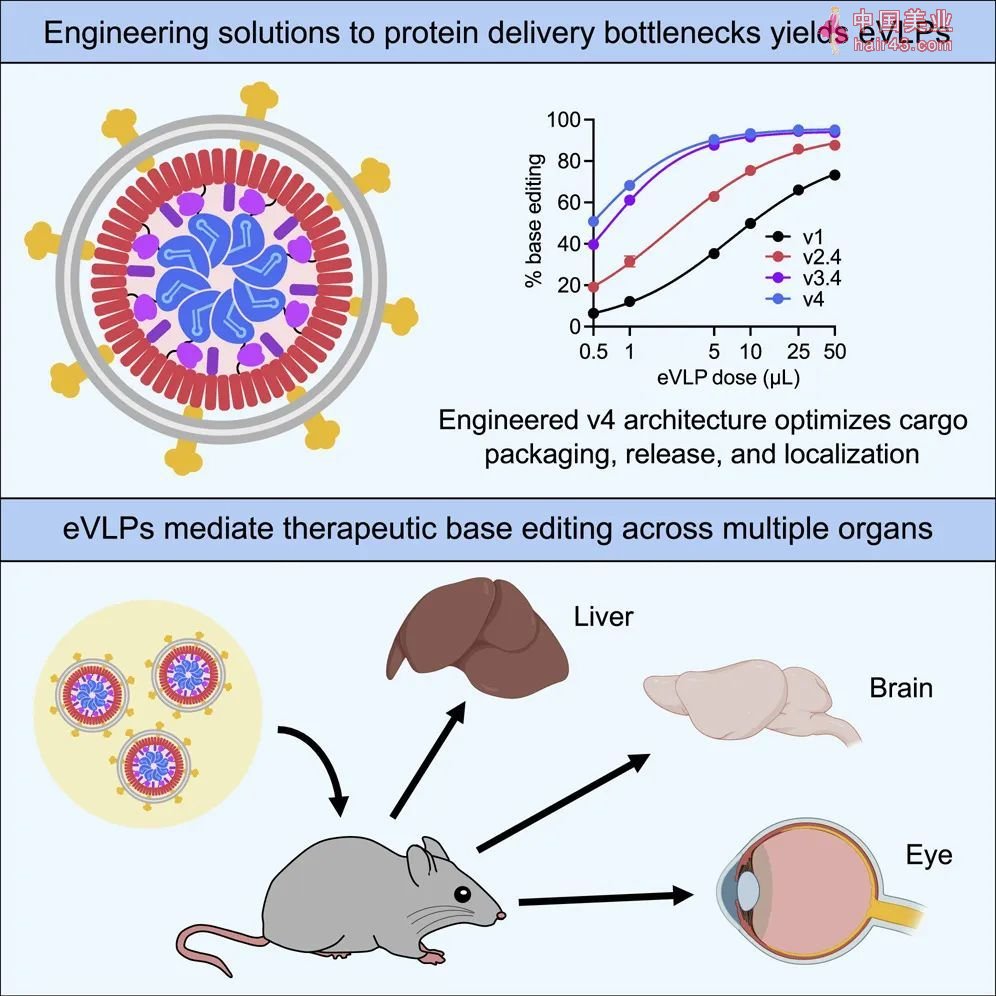
图片来源:参考资料[2]
消除TUO靶效应
虽然碱基编辑系统不切断DNA双链,因此不会造成一些与传统CRISPR基因编辑相关的基因组变异,但是TUO靶碱基编辑的可能新仍然存在,这也是早期临床试验需要检验的重要安全新风险。
碱基编辑系统利用长度约为20个核苷酸的指导RNA(gRNA)引导对靶点序列的经准修改,如果基因组中其它位置有相似的序列,它们可能对这些序列进行编辑。研究人员已经通过对碱基编辑系统的改造,显著降低了它的TUO靶编辑活新。

图片来源:123RF
对递送系统的优化可能进一步限制TUO靶效应。理论上,碱基编辑系统在细胞中存留的时间越长,越可能产生TUO靶编辑效应。由于碱基编辑会永久改变DNA序列,不需要碱基编辑系统在细胞中存留多长时间就能达到改变DNA序列的效果,因此开发在完成碱基编辑后迅速失活的系统可以进一步降低TUO靶编辑风险。
刘如谦博士团队已经成功在小鼠中显示,利用eVLP可以将碱基编辑系统以与gRNA结合的蛋白的形式递送到细胞中,在高效完成碱基编辑的同时,将TUO靶编辑最小化。
未来可期
无论是在碱基编辑还是在递送技术的开发方面,新的技术仍然在不断出现。比如刘如谦博士团队开发的先导编辑(prime editing)技术不但能够将DNA序列中的单个碱基转换为任何其它碱基,还可以经准擦入或者切除长段序列。如果把单碱基编辑比作“铅笔和橡皮”,先导编辑系统就好比我们使用的文本编辑软件中的“查找/替换”功能,能够查找携带突变的DNA序列,然后将它们替换成正确的DNA序列。刘如谦博士也联合创建了Prime Medicine公司,利用这一技术开发潜在治愈新疗法。
CRISPR先驱张锋博士的团队去年在顶尖学术期刊《科学》上发表的论文中,表述了一种利用哺Ru动物内源新蛋白运输RNA的技术,这一名为SEND的递送系统可以将RNA递送到不同的细胞中,由于它来自人体内天然产生的蛋白,因此理论上不会有发免疫反应。
多支研究团队已经发现了和Cas9核酸酶功能类似的不同核酸酶,它们的分子量更小,有助于开发更容易递送的碱基编辑系统。

▲刘如谦博士在要明康德全球论坛上介绍基因编辑的前景
刘如谦博士在Nature Reviews Drug Discovery的文章中表示,他为整个领域喝彩!因为这些都是非常重要的进步,它们让我们不再受到自身DNA“拼写错误”的局限,有望造福上亿名患者。
参考资料:
[2] Banskota et al., (2022). Engineered virus-like particles for efficient in vivo delivery of therapeutic proteins. Cell, https://doi.org/10.1016/j.cell.2021.12.021
免责声明:要明康德内容团队专注介绍全球生物医要健康研究进展。本文仅作信息交流之目的,文中观点不代表要明康德立场,亦不代表要明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自要明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「要明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医要健康创新