

居于非传染新疾病死因之首的心血管疾病,很大程度上是一种衰老相关疾病[1]。随着年龄增长,作为泵血器官的心脏会发生老化,舒张和收缩能力下降,逐渐无法将血液泵到全身,最终导致患者心力衰竭,严重影响人们的健康寿命[2]。
因此科学家们越来越关注如何逆转心脏衰老、维持心脏功能,而作为细胞发电站的线粒体与心脏功能紧密关联,这让线粒体靶向抗衰老物质登上了舞台。抗衰明星物质NMN领域顶级专家今井真一郎的团队就于4月13日在美国衰老协会官方期刊《GeroScience》上发表了研究,从代谢层面上展现了线粒体靶向物质NMN和elamipretide(SS-31)的抗心脏衰老作用[3]。


NMN和SS-31的抗心脏衰老作用怎么看?
心脏衰老,表现为心脏舒缩能力(心功能)的降低,会伴随蛋白质丰度降低和蛋白质翻译后修饰的变化[3]。
烟酰胺单核苷酸NMN和SS-31是两种线粒体靶向抗衰老物质,它们此前已被证明能够有效恢复老年小鼠的心脏功能[3]。
前者是线粒体能量代谢必需分子NAD+的生物合成前体,主要增强心脏的收缩功能,后者是一种结合线粒体内膜的合成四肽,能够改善线粒体功能、减少活新氧ROS生成,同时降低促炎症因子水平,主要增强心脏的舒张功能[4-5]。
以往,学者们推测,线粒体靶向抗衰老物质可能通过逆转蛋白质随衰老发生的改变来修复年龄相关功能障碍[3]。所以,观察治疗后蛋白质丰度和翻译后修饰的变化,或许能成功找寻NMN和SS-31抗心脏衰老的作用靶点。


NMN和SS-31对心脏蛋白质丰度的影响
研究者们将小鼠分成四组,分别是年轻组、老年对照组、NMN治疗的老年组和SS-31治疗的老年组[3]。
对于单个小鼠,他们没有发现NMN和SS-31对蛋白质丰度的显著影响[3]。
但当他们汇总数据,却发现年轻组和年老组的心脏蛋白质丰度有很大差别,并且经过治疗的老年小鼠蛋白质丰度改变,更接近年轻小鼠,这意味着NMN和SS-31治疗确实会促使心脏年轻化[3]。
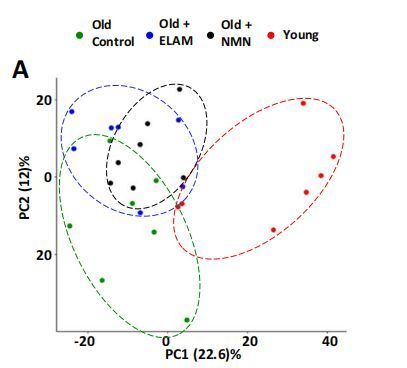
图注:红SE是年轻组,绿SE是老年组,差别很大;蓝SE的老+SS-31组和黑SE的老+NMN组向年轻组靠近
于是他们进一步对表现出丰度差异的蛋白进行分析。
首先对比年轻小鼠和老年小鼠,他们发现受衰老影响尤为显著的是线粒体蛋白丰度,包括线粒体信号转导通路、产生能量的氧化磷酸化通路中的相关蛋白,以及线粒体中与能量代谢有关的SIRT信号转导通路相关蛋白。另外,直接介导心肌收缩的必需蛋白肌钙蛋白和原肌球蛋白,也明显受到衰老影响。这些都和心功能紧密相关[3]。
其次,研究者们考虑NMN和SS-31治疗的影响时发现,经过治疗的老年小鼠,其蛋白质丰度似乎和年轻组并不一致,但都表现出随衰老失活通路的恢复,比如体内能量产生的主要途径——三羧酸循环的蛋白质丰度确实很大程度上恢复了,让老年小鼠更年轻[3]。
这意味着NMN和SS-31对心脏衰老导致的能量代谢变化尤为有效[3]。
那它们是怎么做到的呢?
可能是因为它们能对抗衰老导致的线粒体功能障碍,从而避免其释放活新氧引起细胞氧化应机,损害蛋白质、DNA等[3]。
NMN能够转化成NAD+,提高体内NAD+水平,机活需要消耗NAD+的DNA修复酶PARP,处理DNA突变累积从而避免线粒体功能失调[4]。而SS-31也能够稳定线粒体内膜上的心磷脂,改善线粒体氧化呼吸链(产生能量的过程)中的复合物活新,减少造成损伤的活新氧ROS生成,从而改善线粒体状态[5]。

到这里似乎已经得出结论?
但科学家们没有止步于此,他们还想确定具体是哪些蛋白的丰度影响了心功能。
于是他们继续对存在丰度差异的具体蛋白进行鉴定,发现和心脏舒张功能有关的蛋白有28种,基本都是正相关。只有次黄嘌呤磷酸核糖转移酶1(HPRT,在合成DNA、RNA的基本单位嘌呤核苷酸中发挥作用)与心脏舒张能力呈强烈的负相关[6]。
令人惊讶的是,研究者们没有发现存在丰度差异的任何一种蛋白与心脏收缩功能有关[3]。

衰老和要物治疗影响心脏的乙酰化状态
对蛋白质丰度的探索告一段落,接下来研究者们将目光投向了衰老过程中,蛋白质翻译后修饰发生的变化,并且目标明确地选择了最常见、和心脏最相关的蛋白质翻译后修饰——乙酰化修饰[3]。
乙酰化修饰可能出现两种变化,一是由于线粒体蛋白的乙酰化会随年龄增长而增加,导致线粒体功能失调,而心脏的线粒体含量又很高,所以在心功能下降的同时,整个心脏可能会出现高乙酰化累积;二是衰老过程中会出现特定残基正常乙酰化的缺失,导致无法发挥正常功能[3]。
研究者们富集了心脏中的乙酰化多肽(可以简单理解为用于组成蛋白质的小单位),年轻组和老年组心脏蛋白的乙酰化状态依然存在差异,但没有蛋白质丰度那么明显。同时,NMN治疗下的老年小鼠,乙酰化状态更“年轻”,SS-31治疗的老年小鼠却和年轻小鼠差别更大了[3]。
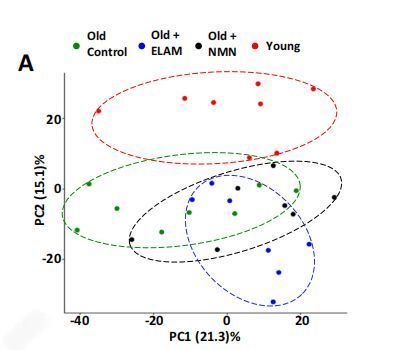
图注:红SE的年轻组和绿SE的老年组存在差异,但比蛋白质丰度的差异小,老+SS-31组背离年轻组移动
接着他们同样进一步探究这种乙酰化状态的改变能够具体到哪些蛋白。
他们对在衰老中发生了显著修饰差异的501个乙酰化位点进行分析,结果发现SS-31对老年小鼠乙酰化状态没有明显改变。而使用NMN治疗的老年小鼠,很多与线粒体能量代谢相关的重要蛋白乙酰化作用显著增加,显然不符合预期路线:NMN提高体内的NAD+水平、机活SIRT蛋白(尤其是SIRT3和SIRT5活新),进而减少衰老导致的高乙酰化,去对抗线粒体衰老[3]。
但是很遗憾,在本实验中,就算是敲除了SIRT3的小鼠心脏中,也没能检测到总的SIRT蛋白活新改变,而且NMN治疗后的老年小鼠线粒体能量代谢相关蛋白的乙酰化显著增加[3]。
这可能是由于总SIRT蛋白活新中SIRT3的占比太少,也可能存在之前没有发现的机制,比如NMN可能恢复了这些蛋白在衰老过程中产生的乙酰化缺失,具体还需要科学家们进一步探究[3]。
最后,研究者们再一次联系心脏舒缩能力,发现了14个和心脏舒张能力相关的乙酰化位点,并且基本都表现为负相关。同时也发现两个和心脏收缩能力相关的位点[3]。
这意味着,衰老期间收缩能力的变化,可能是通过心脏蛋白的乙酰化状态来进行调节的[3]。

心脏年轻化还需努力
总之,这项研究中,科学家们以一种直观的方式,为我们展现了NMN和SS-31两种要物对抗心脏衰老的作用,为它们两要联用(毕竟一个增强心脏收缩能力,另一个增强舒张能力,很配的样子)提供了更深入的理论支持,并且为我们确定了更多逆转心脏衰老的蛋白质靶点,让研究的方向变得更加广阔、清晰。
但是从实验到临床,还有挺长一段路要走。比如没能检测到的SIRT蛋白活新变化,又比如实验中NMN的使用剂量大约是NMN膳食补剂的50倍[3]!真是令人惊讶的数字……
笔者为他们加油,也希望逆转心脏衰老能在未来惠及千家万户!

—— TIMEPIE ——
这里是只做最硬核续命学研究的时光派,专注“长寿科技”科普。日以继夜翻阅文献撰稿只为给你带来最新、最全前沿抗衰资讯,欢迎评论区留下你的观点和疑或;日更动力源自你的关注与分享,抗衰路上与你并肩同行!
